Exploraciones complementarias realizadas al diagnóstico:
- Hemograma: Hb 7,5 g/dl, volumen corpuscular medio (VCM) 70 fl, leucocitos 4,3x109/l, plaquetas 131x109/l.
- Bioquímica: creatinina 2,8 mg/dl, tasa de filtración glomerular (TFG) 18 ml/min, proteínas totales 9,1 g/dl.
- Albúmina: 3 g/dl, calcio corregido 15,1 mg/dl, lactato deshidrogenasa (LDH) 210 UI/l.
- Inmunofijación suero: banda monoclonal IgG kappa.
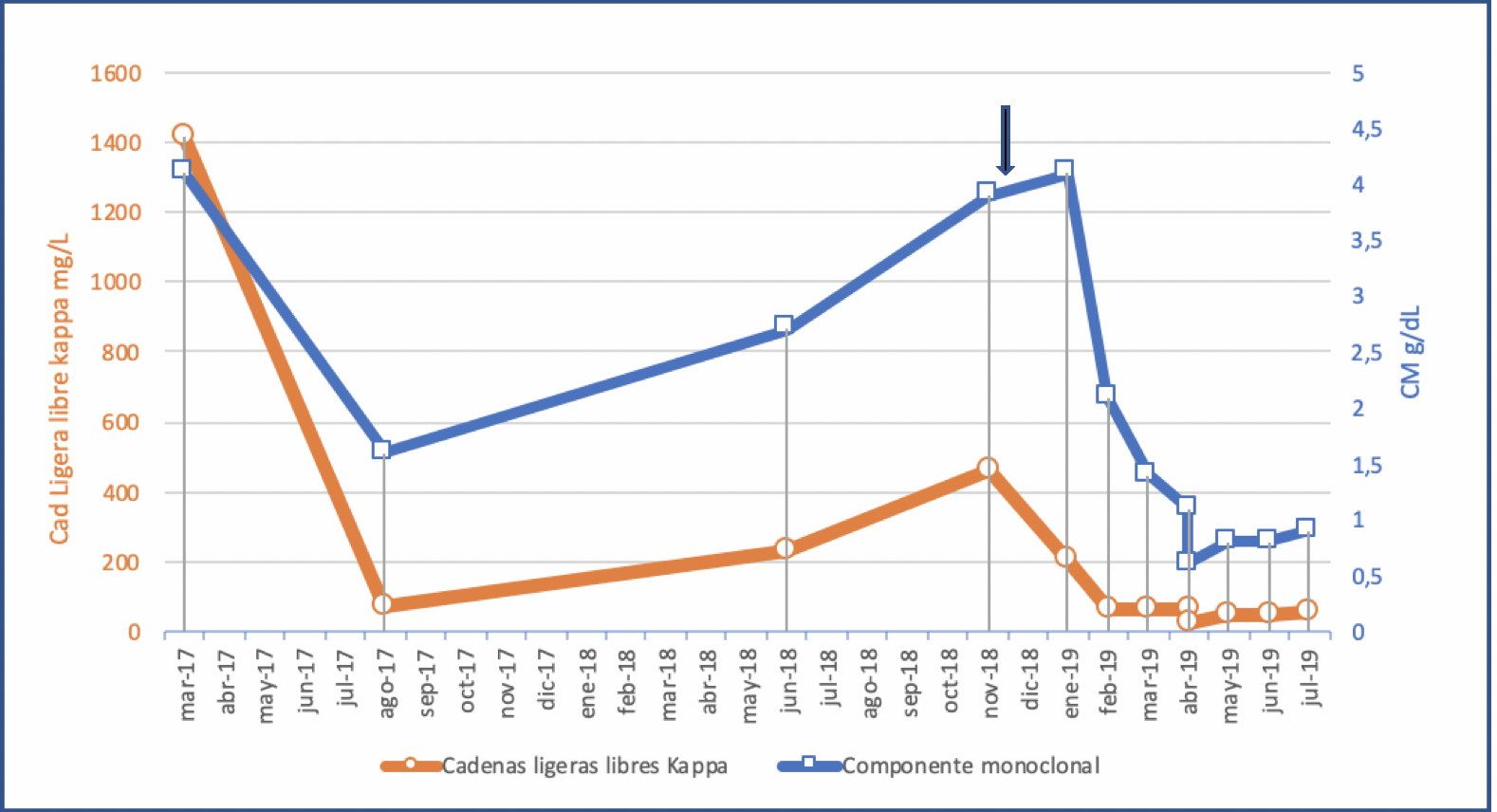
- Proteinograma suero: componente monoclonal (CM) 4,1 g/dl.
- Inmunofijación orina: Bence-Jones kappa, no cuantificable.
- Cuantificación de Ig: IgG 4770 mg/dl, IgA 75 mg/dl, IgM 12 mg/dl.
- Cadenas ligeras libres (CLL) en suero: kappa 1420 mg/l, lambda 58 mg/l, cociente kappa/lambda 24,48.
- Beta-2-microglobulina: 5,9 mg/l.
- Aspirado de médula ósea (AMO): 22 % células plasmáticas de morfología atípica.
- Inmunofenotipo: CD19 negativo, CD38 positivo, CD56 positivo, IgS kappa positivo.
- Hibridación fluorescente in situ (FISH): amplificación 1q positivo. Deleción 17p y reordenamiento IgH negativos.
- Cariotipo: 56,X,-1,+3,+5,+9,+9,+15,+21,+5 mar(5)/ 46 XX(17).
- Tomografía axial computarizada (TAC) toraco-abdominal con contraste intravenoso: fracturas de cuerpos vertebrales D11, D12 y L1.